自10日海关总署发布第53号公告对“6307900010”等19个商品编号项下医疗物资实施出口商品检验新政以来,给目前火热的医疗物资出口带来了更大的不确定性。近两天行业内一直围绕着医疗物资出口法检这一问题争论不休。
海关刚刚印发《海关实施出口医疗物资法定检验工作方案》的通知,即对第53号公告的具体操作做出了权威解释,从而可能一切疑问将尘埃落定!该通知明确:对53号公告所列11类出口法检医疗物资企业通过单一窗口申报报关,不同于其他出口法检商品的是,此次新增法检出口医疗物资采取验证管理方式,无需实施产地检验、报关时无需出口电子底账,企业只需正常申报报关单!
关于《海关实施出口医疗物资法定检验工作方案》的通知内容摘要及解读如下:
针对该通知的摘要及解读
在解读之前,先带大家了解一下“5号公告”里的5类医疗物资和53号公告里的11类(19个商品编码)出口法检医疗物资。
“5号公告”里的5类医疗物资
2020年3月31日,商务部联合海关总署、国家药品监督管理局发布了《商务部 海关总署 国家药品监督管理局 公告(2020年第5号)- 关于有序开展医疗物资出口的公告》(下称“第5号公告”)。第5号公告对于检测试剂、医用口罩等医疗物资的出口,提出了新的申报要求,即出口企业于报关时须提供书面或电子《出口医疗物资声明》,以及出示医疗器械产品注册证书,海关凭以验放出口。该第5号公告自2020年4月1日起实施。
第5号公告适用于5种出口医疗物资,包括新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机和红外体温计。普通民用口罩、消毒液和酒精等尚未落入《医疗器械分类目录》管理,其出口并无《出口医疗物资声明》要求。
上述五种医疗物资,属于《医疗器械分类目录》管理的医疗器械,具体管理类别如下:
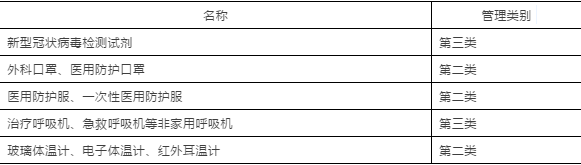
53号公告里的11类出口法检医疗物资
为加强医疗物资出口质量监管,海关总署决定4月10日起对“6307900010”等海关商品编号项下的11类医疗物资实施出口商品检验。
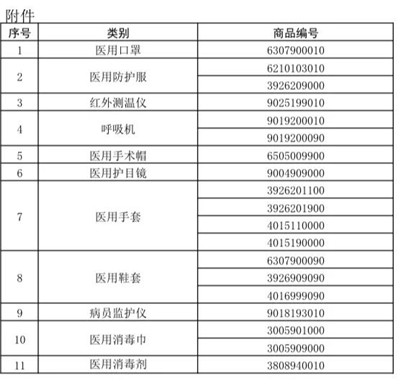
按照该通知要求,对于53号公告规定的11类(19个商品编码)出口法检医疗物资,采取的是验证管理方式,就是不需要做商品品质检验,无需出口电子底账,企业正常申报报关单。
单证提交要求:在三部委发布的“5号公告”里的5类医疗物资,提交医疗器械产品注册证和企业承诺声明;在三部委发布的“5号公告”外的医用物资,企业提交注册证和质量安全承诺书,非医用物资不要求提交注册证和质量安全承诺书。
海关审核要求:三部委5号公告涉及5类医疗物资,而海关53号公告涉及11类医疗物资。其中,4类相同,7类不相同。但都是对于医疗物资的新措施,不是对于非医疗物资的新措施。所以,海关申报系统中并没有对53号公告中的19个HS设置出口商检监管条件。海关采取电子审核加人工审单的方法,处理53号文件涉及的申报单证。涉及53号公告的出口防疫物资申报时,不需要电子底账,数据不走ECIQ系统。
三部委5号公告的4类商品按5号公告要求办理,需提供中国医疗器械产品注册证和企业承诺说明书,不需要做产品法定检验。
对53号公告新增的7类商品,综合业务岗位几乎100%人工审单,发现未放行的可以联系海关审单部门。对非医用的,若没被布控,直接放行;对医用的,需企业提供注册证书(可以是电子扫描件)及出口企业的质量承诺书,有上传的,原则上(被风险布控或者综合业务岗人工审单有疑问的、决定布控除外)予以放行,没有上述注册证书或者出口企业质量保证承诺书的,将可能被布控。
查验资料要求:如果产品涉及医疗物资,企业需提供注册/备案证明和质量安全承诺书。对于现场无法判定或企业提出异议的送实验室检测。该通知明确了“在确定是否为医疗物资时,应根据商品本身特征而非申报用途”。
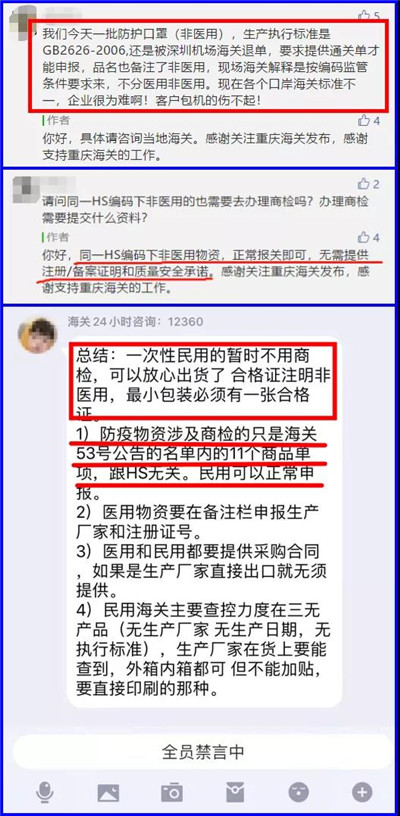
据了解,目前实际操作中,仍然还是按照之前的正常申报,但大概率都会被查验。应该不会被退单,但也不排除目前各地海关对政策理解不同出现偏差,重庆海关发布、12360海关热线反馈如下,出货仍须谨慎。
法检医疗物资出口快速通关检验指南
根据海关总署2020年第53号公告,自4月10日起,对“6307900010”等海关商品编号项下的11类医疗物资实施出口商品检验,共涉及19个HS编码。之前,对出口检测试剂已实施卫生检疫。
一、出口申报
对53号公告所列11类出口法检医疗物资企业通过单一窗口申报报关,不同于其他出口法检商品的是,此次新增法检出口医疗物资一般无需实施产地检验,报关时无需出口电子底账。
(1)对出口法检医疗物资,企业需在报关单商品名称栏填报用途,并注明是否医用,检测试剂需注明是否为新型冠状病毒检测用。
温馨提示:同一HS编码下既有医疗物资又有非医疗物资的,应根据商品本身特征即生产制造标准,确定是否医用。
(2)对三部委“5号公告”所列(含公告后续调整所列)的出口新型冠状病毒检测试剂、医用口罩、医用防护服、呼吸机、红外体温计5类医疗物资,企业向海关报关时,须提供书面或电子声明和我国医疗器械产品注册证书。新冠病毒检测试剂还须提供药监部门出具的出口销售证明。
(3)对其他出口法检医疗物资,企业向海关报关时,应当提供医疗器械产品注册/备案证明和质量安全承诺声明。对无相关证明和承诺声明的,海关将实施严密监管。
(4)对新冠病毒检测试剂,发货人应当申请卫生检疫审批,凭《入/出境特殊物品卫生检疫审批单》通过单一窗口报检,经海关检验合格后,获得电子底账,报关时填写电子底账帐号。
郑重提示:企业必须按规定如实向海关申报,对将医用物资伪报为非医用物资的,依法从重处罚;涉嫌构成犯罪的,移送地方公安机关追究刑事责任。
二、质量安全要求
出口法检医疗物资应当符合进口国(地区)的要求,对进口国(地区)无质量安全标准要求的,应当符合我国质量安全标准。
小工具
医疗物资国内外质量安全标准可登陆“海关总署网站—总署概况—商品检验司—政策法规”栏目查询(不定期更新),访问地址:http://sjs.customs.gov.cn/sjs/zcfg56/index.html
部分国家(地区)防疫物资技术法规和标准要求(第三版),访问地址:http://sjs.customs.gov.cn/sjs/zcfg56/2963129/index.html
我国和国外部分国家(地区)防疫医疗物资质量安全标准和主要项目(第一版),访问地址:http://sjs.customs.gov.cn/sjs/zcfg56/2963129/index.html
三、装运前检验
按照中国和国外政府签订的双边协议,对出口至部分国家和地区的商品需申请实施装运前检验。

企业是出口医疗物资质量安全第一责任人,海关依法实施检验监管。出口属于掺杂掺假、以假充真、以次充好的商品或者以不合格进出口商品冒充合格进出口商品的,将依法依规严厉查处;构成犯罪的,依法追究刑事责任。
厦门汉连物流有限公司具有稳定而优质的全球网络代理资质及报关报检团队,且旗下汉连供应链具有进出口经营权,十几年来长期从事进出口经营代理,在国内疫情爆发期,曾为国内多方提供医疗物资&非医疗物资的进口物流通关服务,在今年2月快速新增了第二类医疗器械经营许可及备案,可为医用类防疫物资提供出口代理。
详情请咨询我司代理出口热线:0592-5608333-118
来源:海运信息




